eISSN 2444-7986
DOI: https://doi.org/10.14201/orl.31902
ARTÍCULO ORIGINAL
EFECTIVIDAD REAL DE LA TERAPIA BIOLÓGICA EN EL TRATAMIENTO DE PACIENTES CON RINOSINUSITIS CRÓNICA CON POLIPOSIS NASOSINUSAL
Real life effectiveness of biologics in the treatment of patients with chronic rhinosinusitis with nasosinusal polyposis
Cristina GARCÍA-GARCÍA; Ithzel VILLARREAL-PATIÑO ; Adriana PARDO-MAZA
; Adriana PARDO-MAZA ; Gabriela BOSCO-MORALES
; Gabriela BOSCO-MORALES ; Estefanía MIRANDA-SÁNCHEZ
; Estefanía MIRANDA-SÁNCHEZ ; Guillermo PLAZA-MAYOR
; Guillermo PLAZA-MAYOR
Hospital Universitario de Fuenlabrada. Hospital Sanitas la Zarzuela. Hospital Nuestra Señora del Rosario. Hospital Universidad Rey Juan Carlos. Madrid. España.
Correspondencia: crisgar223@gmail.com
Fecha de recepción: 15 de enero de 2024
Fecha de aceptación: 23 de abril de 2024
Fecha de publicación: 27 de abril de 2024
Fecha de publicación del fascículo: 20 de junio de 2024
Conflicto de intereses: Los autores declaran no tener conflictos de intereses
Imágenes: Los autores declaran haber obtenido las imágenes con el permiso de los pacientes
Política de derechos y autoarchivo: se permite el autoarchivo de la versión post-print (SHERPA/RoMEO)
Licencia CC BY-NC-ND. Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional
Universidad de Salamanca. Su comercialización está sujeta al permiso del editor
RESUMEN: Introducción y objetivo: El tratamiento de la rinosinusitis crónica con poliposis nasosinusal (RSCcPN) se basa en el uso de corticoterapia local intranasal, ciclos de corticoides sistémicos y cirugía endoscópica nasal. La terapia biológica está ganando cada vez más protagonismo en el tratamiento de esta patología en casos resistentes al tratamiento cásico. El objetivo de este trabajo es determinar la efectividad real de los tratamientos biológicos administrados para la RScPN fuera del ámbito de los ensayos clínicos. Método: Estudio retrospectivo sobre pacientes con RSCcPN y asma en tratamiento con terapia biológica en un hospital universitario. Analizaremos mediante un estudio de Wilcoxon signed-rank la eficacia de los distintos tratamientos biológicos administrados. Resultados: La muestra incluyó 21 pacientes con un seguimiento mínimo de 24 meses. Se evidenció una significación estadistica (p = <0, 001) en cuanto a la mejoría de la sintomatología, a excepción del olfato, así como de una mejoría del Nasal Polyp Score, el SNOT-22 y la escala Lund-Mackay en la TC. De los 21 pacientes, 7 de ellos (33%) han necesitado rescates con tratamiento corticoideo a nivel sistémico. Sin embargo, no hubo que realizar una nueva CENS en ninguno de ellos. Discusión: Los datos obtenidos en este estudio de efectividad en práctica clínica real concuerdan con los obtenidos en ensayos clínicos acerca de la terapia biológica en la RSCcPN. Se han documentado reducciones notables en la carga de enfermedad de RSCcPN de forma objetiva y subjetiva, así como menor necesidad de rescate corticoideo oral o cirugía. Conclusiones: En nuestro estudio se ha corroborado la eficacia de la terapia biológica en prácticamente todos los datos analizados. Sin embargo, no se ha conseguido demostrar la relevancia de un tipo de terapia respecto a otra.
PALABRAS CLAVE: RSCcPNS; terapia biológica; respuesta Th2.
SUMMARY: Introduction and objective: Nowadays, treatment proposals for patients with recurrent sinonasal polyposis are based on the use of local intranasal corticosteroid therapy based on topical inhalers, cycles of systemic corticosteroids and endoscopic nasal surgery. Biological therapy is gaining more and more prominence in the treatment of this pathology. The objective of this work is based on determining which biological treatment of those administered today for this disease is more effective in managing symptoms and in its evolution. Method: Retrospective study of 21 patients with chronic rhinosinusitis with sinonasal polyposis and asthma under treatment with biological therapy at the University Hospital of Fuenlabrada. Using a Wilcoxon signed-rank study, we will analyze the efficacy of the different biological treatments administered. Results: A statistical significance with p = <0, 001 was evidenced in terms of the improvement of the symptoms suffered by the study patients (with the exception of smell) as well as an improvement in the Nasal Polyp Score of 3 points. The Wilconxon test result was statistical significance with p = <0, 001. Discussion: The data obtained in this study agree with those obtained in studies on biological therapy in CRSwNP. Remarkable reductions in the disease burden of CRSwNP have been documented objectively and subjectively. This is consistent with the fact that our patients required fewer reinterventions throughout the procedure. Conclusions: In our study, the efficacy of biological therapy has been corroborated in practically all the data analyzed. However, it has not been possible to demonstrate the relevance of one type of therapy over another.
KEYWORDS: CRSwNP; biological therapy; Th2 respond.
INTRODUCCIÓN
La rinosinusitis crónica (RSC) es una enfermedad inflamatoria que afecta a la nariz y a los senos paranasales entre el 5-10% de la población general. La poliposis nasosinusal (PN) conforma un fenotipo importante dentro de la RSC, con mayor morbilidad y coste en el tratamiento de estos pacientes, presentando una prevalencia del 4% en Europa y EEUU [1]. En España, la prevalencia de rinosinusitis crónica con PN (RSCcPN) es del 3-6% [2]. Esta enfermedad afecta hasta tres veces más al sexo masculino y la clínica suele aparecer alrededor de la cuarta década de la vida [1, 2].
En muchas ocasiones, esta patología suele asociarse con otras principalmente el asma, aunque también pude asociarse con enfermedad respiratoria exacerbada por AINEs [1]. La presencia de RSCcPN se asocia con asma grave en el 70-90% de los casos, lo que modifica el abordaje terapéutico en muchos casos [2].
Numerosos procesos fisiopatológicos relacionados con la presencia de eosinófilos, basófilos y mastocitos, IgE elevada, circulante a nivel sistémico y local, así como la activación de IL-4, IL-5 e IL-13, intervienen en la cascada de señalización de respuestas inflamatorias tipo Th2 que se ha visto involucrada en el 85% de los pacientes diagnosticados con RSCcPN [1-3]. Estos mismos procesos ya fueron descritos previamente en pacientes con diagnóstico de asma.
En la actualidad, las propuestas de tratamiento en pacientes que presentan RSCcPN se basan principalmente en el uso de corticoterapia local mediante inhaladores nasales y ciclos de corticoides sistémicos. Sin embargo, son muchos los pacientes que no responde al uso de corticoides tópicos o que requieren ciclos repetidos de corticoterapia oral. Por otro lado, en aquellos pacientes en los que se demuestra respuesta objetiva a este tipo de tratamientos, no se obtiene realmente una mejoría subjetiva por parte del paciente en síntomas como el olfato. Por lo tanto, se recurre a la cirugía endoscópica nasal (CENS) para la exéresis de los pólipos [1-3]. En muchas ocasiones deben realizarse varias intervenciones quirúrgicas tras el fracaso del tratamiento médico asumiendo el paciente el riesgo de recaída y la necesidad de una nueva intervención.
Con el auge de la denominada medicina personalizada, se han desarrollado en los últimos años terapias biológicas diseñadas para actuar contra la respuesta inflamatoria tipo Th2 [3-6]. Su uso en la RSCcPN ha quedado limitado a ensayos clínicos en marcha para su desarrollo, como es el caso de omalizumab, benralizumab, dupilumab y mepolizumab [4]. Sin embargo, estos tratamientos, en España, al estar incluidos en ficha técnica para el tratamiento del asma grave, han sido también utilizados esporádicamente para la RSCcPN en algunos pacientes con RSCcPN y asma severa hasta diciembre de 2023.
En este estudio analizaremos de manera retrospectiva los pacientes diagnosticados de RSCcPN y asma severa en tratamiento con fármacos biológicos, evaluando en la vida real, cómo ha evolucionado la enfermedad, el requerimiento de otras terapias como corticoides intranasales o sistémicos, la necesidad de CENS y la eventual presencia de complicaciones derivadas de estos fármacos.
MATERIAL Y MÉTODO
Previo aprobado por el CEIm del Hospital Universitario de Fuenlabrada (HUF) en noviembre de 2022, se ha realizado un estudio retrospectivo, en el que se han incluido pacientes con RSCcPN y asma severa que habían iniciado tratamiento con terapia biológica dirigida contra la respuesta inflamatoria Th2 en el Hospital Universitario de Fuenlabrada hasta enero de 2021, con un seguimiento mínimo de 24 meses.
Se ha analizado la evolución clínica de forma tanto subjetiva como objetiva de pacientes tratados co omalizumab (anti-IgE), benralizumab (anti IL-5R), reslizumab (anti IL-5), dupilumab (anti IL-4R/IL-13R) y mepolizumab (anti IL-5).
Para ello, se han recogido las distintas variables demográficas en posible relación con la patología estudiada, así como las comorbilidades de nuestros pacientes. Se analizó el uso del tratamiento corticoideo tópico intranasal y vía oral requerido por los sujetos a estudio, previo al inicio de la terapia biológica elegida y también tras después de iniciarla. Además, se recogió el número de CENS a los que fueron sometidos, tanto previas al inicio del tratamiento biológico como durante el mismo.
Se revisaron los resultados de la encuesta SNOT-22 y las escalas visuales analógicas (EVA) para evaluar la clínica evidenciada por los sujetos en relación a congestión nasal, rinorrea, presión facial y olfato, tanto antes de la terapia como en el momento de recogida de datos del estudio después del inicio de la terapia biológica.
La evaluación clínica se estudió con pruebas objetivas mediante el NPS (Nasal Polyp Score) en la exploración fibroendoscópica y con la clasificación de Lund-Mackay en la tomografía computarizada (TC) de senos paranasales. Se compararon los resultados obtenidos en las exploraciones y pruebas realizadas pre y post tratamiento.
Para realizar el análisis estadístico, se usó la prueba Wilcoxon signed-rank con una significación estadística del 5% y un poder estadístico del 10% en busca de diferencias significativa de las variables recogidas.
RESULTADOS
En total, en el HUF hasta enero de 2021 se inició la administración de tratamientos biológicos contra patología relacionada con una respuesta inflamatoria Th2 a 142 pacientes. De todos ellos, a 96 pacientes se les ha indicado por asma de difícil control, de los cuales 22 pacientes presentaban de forma concomitante RSCcPN. Un paciente falleció en abril de 2021 por causas ajenas a la terapia biológica, por tanto, se excluyó del estudio, dejando una muestra de 21 pacientes con un seguimiento mínimo de 24 meses.
En la Tabla 1 queda registrada la distribución en cuanto a sexo, edad, comorbilidades asociadas y la necesidad de tratamiento corticoideo o quirúrgico.
Tabla 1. Datos demográficos y distribución del tratamiento administrado a los pacientes del estudio.
Variable |
Subvariable |
Resultado |
Sexo |
Hombres Mujeres |
11 10 |
Edad |
|
54 años |
Comorbilidades |
EREA RGE Sensibilización a polen, gramíneas Fumador AOS Rinosinusitis fúngica alérgica |
9 8 7 6 4 1 |
Cirugía pretratamiento |
CENS funcional CENS Radical |
15 6 |
Biológicos |
Mepolizumab Reslizumab Benralizumab Omalizumab Dupilumab |
7 5 5 3 1 |
Terapia corticoidea durante tratamiento biológico |
Tópico Oral |
14 7 |
EREA: enfermedad respiratoria exacerbaba por Aines, RGE: reflujo gastroesofágico, AOS: apnea obstructiva del sueño, CENS: cirugía endoscópica nasosinusal.
Los fármacos biológicos suministrados a estos pacientes se distribuyeron de la siguiente forma: mepolizumab en 7/21 (33%), reslizumab en 5/21 (24%), benralizumab en 5/21 (24%), omalizumab en 3/21 (14%) y dupilumab en un caso (5%) (Tabla 1).
En nuestro estudio, 13 pacientes (61,9%) requirieron cambiar de tratamiento biológico debido a empeoramiento o no mejoría de la clínica asmática, precisando rescates con tratamiento corticoideo o ingresos hospitalarios repetidos. De ellos, en 7 casos (33,3%) cambiaron de omalizumab a otro tratamiento biológico: en 4 a benralizumab y 3 a mepolizumab. Por otro lado, 6 casos (28,5%) cambiaron mepolizumab por otro fármaco: en 5 (33,3%) a reslizumab, en uno (16,6%) a dupilumab, y en dos de ellos (33,3%) cambiaron primero a benralizumab y posteriormente se mantuvieron con reslizumab (Figura 1).
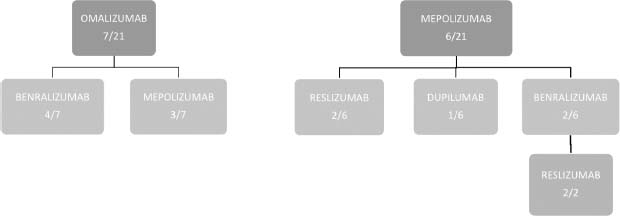
Figura 1. Rotación del tratamiento biológico en los pacientes sometidos al estudio.
La media de tiempo total en tratamiento con biológicos fue de 5 años (mediana: 5 años), aunque todos los pacientes continúan en tratamiento con dichos fármacos tras la finalización del estudio en diciembre de 2023. El tiempo medio de tratamiento con cada biológico se distribuyó de la siguiente forma: la media de meses en tratamiento con omalizumab fue de 7 años (mediana: 8), en el caso de mepolizumab fue de 4 años (mediana: 4 años), para reslizumab una media de 3 años (mediana: 3 años), para benralizumab 4 años (mediana: 4 años) y para dupilumab 2 años.
Del total de la serie, sólo dos pacientes presentaron efectos adversos leves (9,5%), ambos en tratamiento con benralizumab. Uno de ellos presenta cefaleas leves y hormigueos en miembros superiores tras administración, pero no requirió cambio en su terapia biológica. Sin embargo, otro paciente presentó sudoraciones y náuseas tras la administración de este fármaco siendo necesario cambiarlo por reslizumab.
El SNOT-22 previo al tratamiento con biológicos obtuvo una media de 76 puntos (Figura 2), la cual se redujo en 46 puntos tras el tratamiento, siendo la mejoría estadísticamente significativa. Mediante escalas EVA, la sintomatología de los pacientes antes y después del tratamiento mejoró de forma significativa en 4 de los 5 síntomas estudiados (Tabla 2 y Figura 3). Así, para la obstrucción nasal se obtuvo una mejoría de 8 a 4 puntos, de forma significativa, una mejoría que referían el 86% de los pacientes. Para el olfato, se pasó de 4 a 6 puntos, una mejoría del olfato que refirieron el 76% de los pacientes, pero no estadísticamente significativa.
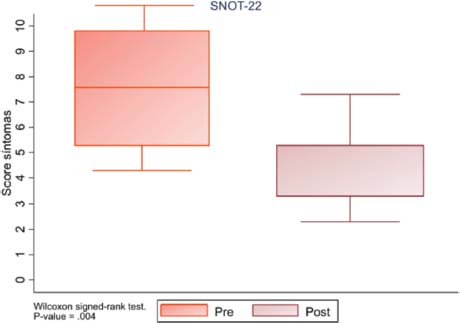
Figura 2. Diagrama de caja y bigotes, mejoría del SNOT-22 tras el tratamiento biológico, con una p significativamente estadística menor a 0,001.
Tabla 2. Análisis estadístico de las variables a estudio.
|
Media prebiológico |
Media postbiológico |
p estadística |
NPS |
6 |
2 |
<0,001 |
Lund-Mckay |
12 |
6 |
<0,001 |
SNOT-22 |
76 |
40 |
<0,001 |
Obstrucción nasal |
7 |
4 |
<0,001 |
Congestión nasal |
7 |
4 |
<0,001 |
Olfato |
5 |
5 |
0,063 |
Rinorrea |
6 |
4 |
<0,001 |
Presión facial |
4 |
3 |
0,004 |
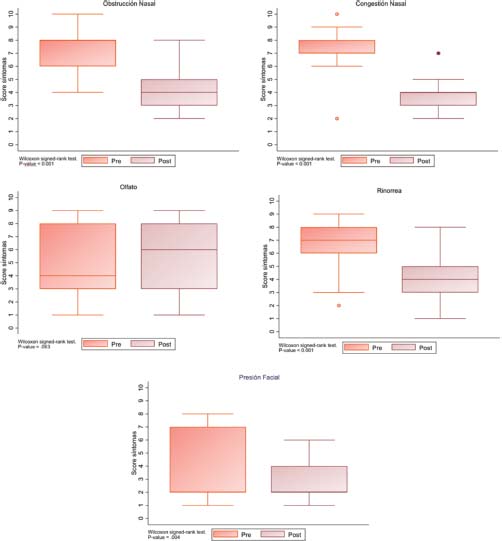
Figura 3. Diagrama de caja y bigotes, mejoría en las escalas VAS tras el tratamiento biológico, con una p significativamente estadística menor a 0,001.
En cuanto al NPS, la media de se redujo de 5 a 2 puntos, una diferencia estadísticamente significativa (p = <0, 001) (Figura 4 y Tabla 2). Analizando la clasificación de Lund-Mackay antes del inicio de la terapia biológica y posterior a la misma, varió de 10 a 6 puntos, de nuevo una diferencia estadísticamente significativa (p = <0, 001). Sin embargo, no se demostró una diferencia estadísticamente significativa entre los distintos fármacos (Figura 5).
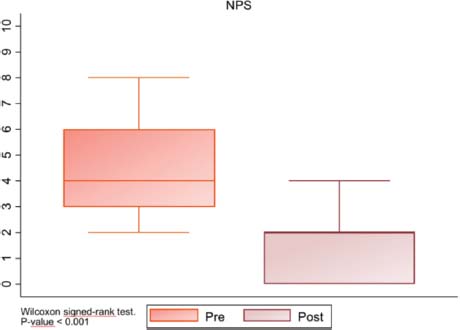
Figura 4. Diagrama de caja y bigotes, mejoría del NPS tras el tratamiento biológico, con una p significativamente estadística menor a 0,001.
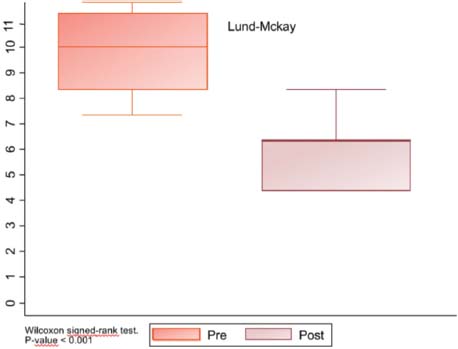
Figura 5. Diagrama de caja y bigotes, mejoría de la clasificación de Lund McKay tras el tratamiento biológico, con una p significativamente estadística menor a 0,001.
De los 21 pacientes, 7 de ellos (33%) han necesitado rescates con tratamiento corticoideo a nivel sistémico. Sin embargo, no hubo que realizar una nueva CENS en ninguno de ellos, a pesar de que todos habían sido operados más de una vez previamente al inicio del tratamiento biológico.
DISCUSIÓN
Aproximadamente, hasta un tercio de los pacientes con RSCcPNS padecen mal control de la enfermedad con tratamientos convencionales [1,2]. Debido a la base inflamatoria tipo Th2 que tiene esta enfermedad, los fármacos biológicos, desarrollados inicialmente para el asma grave o la dermatitis atópica, se han aplicado con éxito a pacientes con RSCcPNS [3-6], Recientemente se han concluido ensayos clínicos de fase III para dupilumab [7], omalizumab [8] o mepolizumab [9], con muy buenos resultados a largo plazo, como se refleja en varias revisiones y metanálisis [4,5,10-15].
En este estudio hemos podido comprobar que la terapia biológica es efectiva en el tratamiento de la sintomatología de pacientes con RSCcPNS y asma grave en situación real, fuera del entorno de un ensayo clínico. Hemos obtenido resultados estadísticamente significativos en prácticamente todas las variables analizadas que interfieren en la vida de nuestros pacientes como son la congestión nasal, la obstrucción nasosinusal, la rinorrea o la presión facial. Además, sólo un 33% de nuestros pacientes han necesitado rescates con tratamiento corticoideo a nivel sistémico, a pesar de padecer asma grave. Así mismo, debemos destacar que ningún paciente precisó de una nueva CENS.
Estos resultados en la vida real coinciden con los publicados por otros autores en numerosos estudios en los últimos dos años [16-30]. Algunos trabajos han intentado comparar la efectidad real de diferebtes anticuerpos monoclonales [16-18]. Así, Haxel et al. [16] han analizado la efectividad del dupilumab y el omalizumab en la RSCcPNS y asma severa sobre 49 y 21 pacientes respectivamente. Observaron una mejoría en el NPS, en los parámetros de calidad de vida y en la función olfatoria en dos tercios de los pacientes con un seguimiento de 12 meses. De forma similar, una comparación en vida real de la efectividad de benralizumab, mepolizumab y omalizumab en pacientes con RSCcPNS y asma severa concomitante fue realizada por Tiotiu et al. [17] incluyendo 16 casos tratados con benralizumab, 21 con mepolizumab y 35 con omalizumab con un seguimiento de 6 meses. Concluyeron que benralizumab y mepolizumab fueron más efectivos en el control del NPS y el recuento de eosinófilos en sangre, si bien los tres anticuerpos monoclonales mejoraron de manera global los síntomas nasales y de asma. Gerstacker y su grupo [18] realizaron un estudio retrospectivo para evaluar la eficacia de los biológicos en pacientes con RSCcPNS en un escenario de la vida real, demostrando una mejoría en la calidad de vida de los pacientes, síntomas, tamaño polipoideo, con raras complicaciones. Nuestra serie muestra similares resultados, con un seguimiento mayor, a dos años.
Analizando cada biológico por separado, para el mepolizumab hay dos trabajos en vida real [19,20]. Detoraki et al. [19] evaluaron el mepolizumab en 44 pacientes con RSCcPNS y asma eosinofílica severa. Hallaron una mejoría significativa en los síntomas nasosinusales y pulmonares, reduciendo el NPS, SNOT-22 y el porcentaje de eosinófilos en las citologías nasales. Domínguez et al. [20] realizaron un estudio en un centro retrospectivo sobre 55 pacientes con RSCcPNS y asma severa en donde objetivaron una mejoría significativa en NPS, en EVA de síntomas, en el Asthma Control Test (ACT), en el óxido nítrico exhalado, en el recuento de eosinófilos en sangre y en la necesidad de administración de prednisona oral tras 6 meses de tratamiento con mepolizumab. Todos los parámetros estudiados mostraron una mejoría notable, dando como resultado un incremento destacado en la calidad de vida de los pacientes con RSCcPNS independientemente de la presencia o ausencia de asma o de la EREA (enfermedad respiratoria exacerbada por aspirina).
Más numerosos son los trabajos sobre dupilumab en práctica clínica real [21-29]. Todos ellos demostraron un progreso adecuado con respecto a los cuestionarios de calidad de vida y el NPS en pacientes con RSCcPNS y asma. Sin embargo, destacan la necesidad de monitorización a corto y largo plazo de la elevación de los eosinófilos en sangre. La Mantia et al. [26] destacaron además el efecto del dupilumab en el olfato, siendo la mejoría claramente más rápida en los pacientes tratados con dicho biológico que en los pacientes con tratamiento corticoideo, independientemente de la severidad de la inflamación tipo 2, del volumen de los pólipos y de la sintomatología subjetiva del paciente. Galletti et al. [29] realizaron un estudio sobre la efectividad y la seguridad del dupilumab en 170 pacientes con RSCcPNS seguidos durante 12 meses, insistiendo en que dicho tratamiento monoclonal debe ser un siempre asociado a una terapia corticoidea intranasal para lograr el efecto deseado con respecto a la mejora en la calidad de vida, severidad de los síntomas, tamaño polipoideo y olfato.
Respecto al omalizumab, Maza et al. [30] han presentado una serie retrospectiva sobre 55 pacientes con RSCcPNS y asma con una respuesta notable al biológico pasados 2 años de inicio del tratamiento. Objetivaron una mejoría temprana en los cuestionarios de calidad de vida, escalas de síntomas, NPS y SNOT 22. Dividieron la muestra en cuatro grupos, siendo superior la respuesta en los pacientes que habían sido operados de CENS al menos una vez en los 10 años previos al tratamiento con omalizumab.
En nuestro estudio, en un primer momento, se quiso determinar la existencia de diferencias en cuanto a la mejoría clínica, radiológica y física de nuestros pacientes en función del tratamiento biológico recibido. Sin embargo, muchos de estos pacientes habían recibido diferentes terapias biológicas a lo largo de su enfermedad para controlar la clínica asmática, siendo frecuente la necesidad de cambiar uno por otro, como refleja la literatura [31,32].
Brkic et al. [31] estudiaron una muestra de 195 pacientes con RSCcPNS o EREA tratados con biológicos donde el 12% de la muestra necesito un cambio de tratamiento por mal control de su sintomatología. Esto se reflejó en una mejoría del control de su patología a largo plazo. La gran mayoría de ellos (73,9%) requirió un cambio de omalizumab a dupilumab, resultados similares a los de nuestro estudio [31,32].
Una vez demostrada la efectividad en práctica clínica real de los biológicos en la RSCcPNS, la siguiente pregunta sería determinar qué tratamiento biológico presenta mejores resultados. En nuestro estudio no pudimos hallar diferencias entre ellos. Hasta la fecha, tampoco hay trabajos prospectivos que comparen en el mismo estudio diferentes tratamientos biológicos en pacientes con RSCcPN. Existen cuatro revisiones sistemáticas y metaanálisis que intentan buscar el mejor biológico [12-15]. Agache et al. [12] realizaron una revisión sistemática para evaluar la eficacia y seguridad de los distintos tratamientos biológicos en la RSCcPNS, hallando que dupilumab también obtuvo los mejores resultados, tanto la mejoría de la calidad de vida de los pacientes como en el uso de tratamiento corticoide de rescate o sobre la necesidad de cirugías de rescate, con un buen perfil de seguridad. Omalizumab también mostró buenos resultados, aunque el número de efectos adversos presentados con este fármaco fue mayor, mientras que reslizumab y mepolizumab aun presentan resultados inciertos según este análisis [14].
Chong et al. [13] realizaron una revisión bibliográfica para la agencia Cochrane acerca del tratamiento con biológicos en la RSC, donde analizaron 10 metanálisis concluyendo que el tratamiento con biológicos obtiene una tasa de respuesta del 50-70%, aunque se desconoce etodavía l perfil ideal de pacientes que se beneficien de este tipo de tratamiento. No se hallaron diferencias significativas de nuevo entre los distintos fármacos y se plantea la duda acerca de la efectividad de este tratamiento en pacientes con RSCcPNS menos grave.
El metanálisis más citado es publicado por Oykhman et al. [14] incluyendo 29 ensayos cínicos y 3461 sujetos. Determinaron que el tratamiento con biológicos en la RSCcPN mejora los resultados de los pacientes, con diferencias clínicamente importantes en los efectos entre los agentes, obteniendo dupilumab mejores resultados, especialmente en la indicación de cirugía de rescate, que se redujo en un 216% con dupilumab, 212% con mepolizumab y 27% con omalizumab. De igual manera, Papacharalampous et al. [15] realizaron una revisión sistemática que incluyó 37 estudios para valorar la eficacia en el tratamiento de la RSCcPNS con omalizumab, dupilumab y mepolizumab. Dupilumab fue el fármaco con mejores resultados, aunque debido a la diferencia metodológica de los estudios, la evidencia científica demostrada aun no es lo suficientemente fuerte.
Entre las limitaciones de nuestro estudio, debemos destacar que se trata de un estudio retrospectivo, con una muestra unicéntrica de tamaño limitado. Además, todos los pacientes padecían asma severo, por lo que no representan una muestra homogénea de pacientes con
RSCcPN, sino un grupo seleccionado.
CONCLUSIONES
La terapia biología en pacientes con RSCcPN ha supuesto una revolución en los últimos años, ya que se ha demostrado que producen una mejoría clínica significativa.
En nuestro estudio se ha corroborado esta efectividad en clínica real tanto en las escalas usasas como SNOT-22, como en el tamaño de los pólipos en NPS o en la TC. Además, sólo un tercio de los pacientes precisaron rescates con corticoides orales y ninguno de los pacientes necesitó de una nueva CENS pasados al menos dos años de seguimiento.
BIBLIOGRAFÍA
1.Fokkens WJ, Lund VJ, Hopkins C, Hellings PW, Kern R, Reitsma S, et al. European Position Paper on Rhinosinusitis and Nasal Polyps 2020. Rhinology. 2020;58(Suppl S29):1-464. https://doi.org/10.4193/Rhin20.600
2.Alobid I, Colás C, Castillo JA, Arismendi E, Del Cuvillo A, Gómez-Outes A, et al. POLINA group. Spanish Consensus on the Management of Chronic Rhinosinusitis With Nasal Polyps (POLIposis NAsal/POLINA 2.0). J Investig Allergol Clin Immunol. 2023;33(5):317-331. https://doi.org/10.18176/jiaci.0910
3.Fokkens WJ, Lund V, Bachert C, Mullol J, Bjermer L, Bousquet J, et al. EUFOREA consensus on biologics for CRSwNP with or without asthma. Allergy. 2019;74(12):2312-2319. https://doi.org/10.1111/all.13875
4.Bachert C, Desrosiers MY, Hellings PW, Laidlaw TM. The Role of Biologics in Chronic Rhinosinusitis with Nasal Polyps. J Allergy Clin Immunol Pract. 2021;9(3):1099-1106. https://doi.org/10.1016/j.jaip.2020.11.017
5.Bachert C. Biologics in chronic rhinosinusitis with nasal polyps. Zhang L, Bachert C, editors. Chronic Rhinosinusitis: The Mucosal Concept. Springer Nature Singapore. 2022:411-21.
6.Borish L, Cohen NA, Chupp G, Hopkins C, Wagenmann M, Sousa AR, et al. Evaluating enrollment and outcome criteria in trials of biologics for chronic rhinosinusitis with nasal polyps. Ann Allergy Asthma Immunol. 2022;129(2):160-168. https://doi.org/10.1016/j.anai.2022.04.004
7.Bachert C, Han JK, Desrosiers M, Hellings PW, Amin N, Lee SE, et al. Efficacy and safety of dupilumab in patients with severe chronic rhinosinusitis with nasal polyps (LIBERTY NP SINUS-24 and LIBERTY NP SINUS-52): results from two multicentre, randomised, double-blind, placebo-controlled, parallel-group phase 3 trials. Lancet. 2019;394(10209):1638-1650. https://doi.org/10.1016/S0140-6736(19)31881-1
8.Gevaert P, Omachi TA, Corren J, Mullol J, Han J, Lee SE, et al. Efficacy and safety of omalizumab in nasal polyposis: 2 randomized phase 3 trials. J Allergy Clin Immunol. 2020; 146(3):595-605. https://doi.org/10.1016/j.jaci.2020.05.032
9.Han JK, Bachert C, Fokkens W, Desrosiers M, Wagenmann M, Lee SE, et al. SYNAPSE study investigators. Mepolizumab for chronic rhinosinusitis with nasal polyps (SYNAPSE): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Respir Med. 2021; 9(10):1141-1153. https://doi.org/10.1016/S2213-2600(21)00097-7
10. Bachert C, Gevaert P, Hellings P. Biotherapeutics in Chronic Rhinosinusitis with and without Nasal Polyps. J Allergy Clin Immunol Pract. 2017;5(6):1512-1516. https://doi.org/10.1016/j.jaip.2017.04.024
11. Patel GB, Peters AT. The Role of Biologics in Chronic Rhinosinusitis With Nasal Polyps. Ear Nose Throat J. 2021;100(1):44-47. https://doi.org/10.1177/0145561320964653
12. Agache I, Song Y, Alonso-Coello P, Vogel Y, Rocha C, Solà I, et al. Efficacy and safety of treatment with biologicals for severe chronic rhinosinusitis with nasal polyps: A systematic review for the EAACI guidelines. Allergy. 2021;76(8):2337-2353. https://doi.org/10.1111/all.14809
13. Chong LY, Piromchai P, Sharp S, Snidvongs K, Webster KE, Philpott C, et al. Biologics for chronic rhinosinusitis. Cochrane Database Syst Rev. 2021;3(3):CD013513. https://doi.org/10.1002/14651858.CD013513.pub3
14. Oykhman P, Paramo FA, Bousquet J, Kennedy DW, Brignardello-Petersen R, Chu DK. Comparative efficacy and safety of monoclonal antibodies and aspirin desensitization for chronic rhinosinusitis with nasal polyposis: A systematic review and network meta-analysis. J Allergy Clin Immunol. 2022;149(4):1286–95. http://dx.doi.org/10.1016/j.jaci.2021.09.009
15. Papacharalampous GX, Constantinidis J, Fotiadis G, Zhang N, Bachert C, Katotomichelakis M. Chronic rhinosinusitis with nasal polyps (CRSwNP) treated with omalizumab, dupilumab, or mepolizumab: A systematic review of the current knowledge towards an attempt to compare agents' efficacy. Int Forum Allergy Rhinol. 2024;14(1):96-109. https://doi.org/10.1002/alr.23234
16. Haxel BR, Hummel T, Fruth K, Lorenz K, Gunder N, Nahrath P, Cuevas M. Real-world-effectiveness of biological treatment for severe chronic rhinosinusitis with nasal polyps. Rhinology. 2022;60(6):435-443. https://doi.org/10.4193/Rhin22.129
17. Tiotiu A, Mendez-Brea P, Ioan I, Romero-Fernandez R, Oster JP, Hoang TC, et al. Real-Life Effectiveness of Benralizumab, Mepolizumab and Omalizumab in Severe Allergic Asthma Associated with Nasal Polyps. Clin Rev Allergy Immunol. 2023;64(2):179-192. https://doi.org/10.1007/s12016-022-08938-w
18. Gerstacker K, Ketterer MC, Jakob TF, Hildenbrand T. Real Life Observational Study of Treatment Success of Monoclonal Antibodies for Refractory Chronic Rhinosinusitis with Nasal Polyps. J Clin Med. 2023;12(13):4374. https://doi.org/10.3390/jcm12134374
19. Detoraki A, Tremante E, D'Amato M, Calabrese C, Casella C, Maniscalco M, et al. Mepolizumab improves sino-nasal symptoms and asthma control in severe eosinophilic asthma patients with chronic rhinosinusitis and nasal polyps: a 12-month real-life study. Ther Adv Respir Dis. 2021;15. https://doi.org/10.1177/17534666211009398
20. Domínguez-Sosa MS, Cabrera-Ramírez MS, Marrero-Ramos MDC, Dávila-Quintana D, Cabrera-López C, Carrillo-Díaz T, et al. Real-Life Effectiveness of Mepolizumab in Refractory Chronic Rhinosinusitis with Nasal Polyps. Biomedicines. 2023;11(2):485. https://doi.org/10.3390/biomedicines11020485
21. Kilty SJ, Lasso A. Canadian real-world study of access and clinical results using dupilumab for chronic rhinosinusitis with polyps. J Otolaryngol Head Neck Surg. 2022;51(1):17. https://doi.org/10.1186/s40463-022-00570-0
22. Book R, Eligal S, Tal Y, Eliashar R. Biological Treatment for Uncontrolled Chronic Rhinosinusitis with Nasal Polyps: Preliminary Real-World Results from a Tertiary Medical Center. J Clin Med. 2023;12(11):3671. https://doi.org/10.3390/jcm12113671
23. Boscke R, Heidemann M, Bruchhage KL. Dupilumab for chronic rhinosinusitis with nasal polyps: real-life retrospective 12-month effectiveness data. Rhinology. 2023;61(3):203-213. https://doi.org/10.4193/Rhin22.469
24. Albrecht T, Sailer MM, Capitani F, van Schaik C, Löwenheim H, Becker S. Real-world evidence for the effectiveness and safety of dupilumab in patients with CRSwNP after 1 year of therapy. World Allergy Organ J. 2023;16(5):100780. https://doi.org/10.1016/j.waojou.2023.100780
25. Mocellin D, Ioppi A, Gaglio G, Pennacchi A, Bertolini M, Tirrito A, et al. Severe chronic rhinosinusitis treated with dupilumab, a real-life analysis of early effectiveness. Eur Rev Med Pharmacol Sci. 2023;27(15):7324-7336. https://doi.org/10.26355/eurrev_202308_33304
26. La Mantia I, Grigaliute E, Ragusa M, Cocuzza S, Radulesco T, Saibene AM, et al. Effectiveness and rapidity on olfatory fuction recovery in CRS patients treated with Dupilumab: a real life prospective controlled study. Eur Arch Otorhinolaryngol. 2024;281:219-226. https://doi.org/10.1007/s00405-023-08184-6
27. Campion NJ, Brugger J, Tu A, Stanek V, Brkic FF, Bartosik TJ, Liu DT, et al. The "real life" efficacy of dupilumab is independent of initial polyp size and concomitant steroids in CRSwNP. J Otolaryngol Head Neck Surg. 2023;52(1):56. https://doi.org/10.1186/s40463-023-00663-4
28. De Corso E, Pasquini E, Trimarchi M, La Mantia I, Pagella F, Ottaviano G, et al. Dupireal Italian Study Group. Dupilumab in the treatment of severe uncontrolled chronic rhinosinusitis with nasal polyps (CRSwNP): A multicentric observational Phase IV real-life study (DUPIREAL). Allergy. 2023;78(10):2669-2683. https://doi.org/10.1111/all.15772
29. Galletti C, Ragusa M, Sireci F, Ciodaro F, Barbieri MA, Giunta G, et al. Dupilumab in chronic rhinosinusitis with nasal polyps: Real life data in a multicentric Sicilian experience. Am J Otolaryngol. 2023;45(1):104106. https://doi.org/10.1016/j.amjoto.2023.104106
30. Maza-Solano J, Callejon-Leblic A, Martin-Jimenez D, Moreno-Luna R, Gonzalez-Garcia J, Cuvillo A, et al. Omalizumab Treatment in Uncontrolled Asthma and CRSwNP Patients, with Previous Endoscopic Sinus Surgery, to Improve Quality of Life and Endoscopic Outcomes: a Two-Year Real-Life Study. Curr Allergy Asthma Rep. 2023;23(10):555-566. https://doi.org/10.1007/s11882-023-01106-w
31. Brkic FF, Liu DT, Klimbacher R, Campion NJ, Bartosik TJ, Vyskocil E, et al. Efficacy and safety of switching between biologics in chronic rhinosinusitis with nasal polyps or N-ERD. Rhinology. 2023;61(4):320-327. https://doi.org/10.4193/Rhin22.408
32. Nagase H, Suzukawa M, Oishi K, Matsunaga K. Biologics for severe asthma: The real-world evidence, effectiveness of switching, and prediction factors for the efficacy. Allergol Int. 2023;72(1):11-23. https://doi.org/10.1016/j.alit.2022.11.008